pandèmia mundial
Pfizer vol començar a distribuir la vacuna al desembre als Estats Units
La farmacèutica diu que pot fabricar 50 milions de dosis de la vacuna contra la Covid
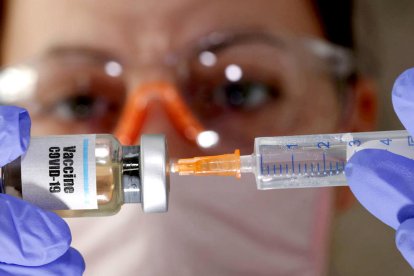
Pfizer vol començar a distribuir la vacuna al desembre als Estats Units
La farmacèutica Pfizer i la seva sòcia alemanya, BioNTech, demanen a l’agència reguladora del medicament dels Estats Units, l’FDA, que els autoritzi d’emergència per començar a distribuir la vacuna contra la Covid-19. La farmacèutica assegura que si rep l’autorització de l’FDA podrà començar a vacunar la població de risc nord-americana a partir del desembre.
Pfizer assegura que té infraestructura potencial per fabricar 50 milions de dosis a tot el món abans d’acabar l’any i 1.300 milions de dosis més l’any 2021. Però ha de fer front al principal punt dèbil de la seva vacuna: s’ha de conservar a temperatures inferiors als 70 graus sota zero.
Aquesta és la primera vacuna contra la Covid que demana una autorització de l’organisme regulador dels EUA. L’Agència d’Aliments i Medicaments (FDA) haurà de revisar almenys dos mesos de les dades de resposta dels voluntaris que han testat la vacuna i certificar que és segura per a infants i persones d’edat avançada.
La presentació a l’FDA es basa en els resultats de la fase 3 de l’assaig clínic de la vacuna, que va començar als Estats Units el 27 de juliol i va inscriure més de 43.000 voluntaris.
L’anàlisi final de l’assaig va trobar que la vacuna contra el coronavirus és el 95% efectiva en la prevenció d’infeccions, fins i tot en els adults més grans, i que no ha causat problemes seriosos de seguretat, segons van anunciar Pfizer i BioNTech aquesta setmana. La presentació també inclou dades de seguretat sobre uns 100 nens d’entre 12 i 15 anys.
Prop del 42% dels participants globals i el 30% dels participants estatunidencs en l’estudi de la fase 3 tenen orígens racials i ètnics diversos, van assegurar les empreses en un comunicat de premsa, i el 41% dels participants globals i el 45% dels estatunidencs tenen entre 56 i 85 anys.
Pfizer i BioNTech treballen també per aconseguir l’aprovació de la seva vacuna amb els reguladors d’Austràlia, el Canadà, el Japó, com també la Unió Europea i el Regne Unit.
ESTUDI
La fase 3 de l’assaig clínic va començar el 27 de juliol i va inscriure més de 43.000 voluntaris. S’ha demostrat el 95% d’efectivitat de la vacuna.
Pfizer i BioNTech treballen per aconseguir l’aprovació amb els reguladors d’Austràlia, el Canadà, el Japó, la Unió Europea i el Regne Unit.